
Cargando...
¿Qué puedo hacer?
tipo de documento Lecciones

A pesar de que átomo significa ‘indivisible’, en realidad está formado por varias partículas subatómicas. El átomo contiene protones, neutrones y electrones, con la excepción del átomo de hidrógeno-1, que no contiene neutrones, y del catión hidrógeno o hidrón, que no contiene electrones. Los protones y neutrones del átomo se denominan nucleones, por formar parte del núcleo atómico.

El electrón es la partícula más ligera de las que componen el átomo, con una masa de 9,11 · 10−31 kg. Tiene una carga eléctrica negativa, cuya magnitud se define como la carga eléctrica elemental, y se ignora si posee subestructura, por lo que se considera una partícula elemental. Los protones tienen una masa de 1,672 · 10−24 g, 1836 veces la del electrón, y una carga positiva opuesta a la de este. Los neutrones tienen una masa de 1,69 · 10−27 kg, 1839 veces la del electrón, y no poseen carga eléctrica.
Las masas de ambos nucleones son ligeramente inferiores dentro del núcleo, debido a la energía potencial del mismo, y sus tamaños son similares, con un radio del orden de 8 · 10−16 m o 0,8 femtómetros (fm).
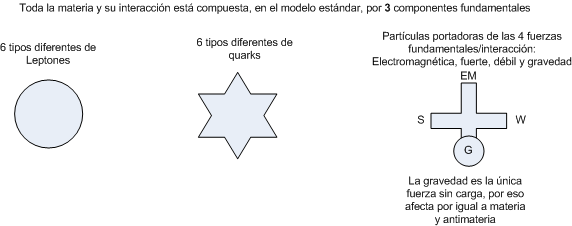
El protón y el neutrón no son partículas elementales, sino que constituyen un estado ligado de quarks u y d, partículas fundamentales recogidas en el modelo estándar de la física de partículas, con cargas eléctricas iguales a +2/3 y −1/3 respectivamente, respecto de la carga elemental. Un protón contiene dos quarks u y un quark d, mientras que el neutrón contiene dos d y un u, en consonancia con la carga de ambos. Los quarks se mantienen unidos mediante la fuerza nuclear fuerte, mediada por gluones —del mismo modo que la fuerza electromagnética está mediada por fotones—. Además de estas, existen otras partículas subatómicas en el modelo estándar: más tipos de quarks, leptones cargados (similares al electrón), etc.
El núcleo atómico
Los protones y neutrones de un átomo se encuentran ligados en el núcleo atómico, en la parte central del mismo. El volumen del núcleo es aproximadamente proporcional al número total de nucleones, el número másico A, lo cual es mucho menor que el tamaño del átomo, cuyo radio es del orden de 105 fm o 1 ángstrom (Å). Los nucleones se mantienen unidos mediante la fuerza nuclear, que es mucho más intensa que la fuerza electromagnética a distancias cortas, lo cual permite vencer la repulsión eléctrica entre los protones.

Los átomos de un mismo elemento tienen el mismo número de protones, que se denomina número atómico y se representa por Z. Los átomos de un elemento dado pueden tener distinto número de neutrones: se dice entonces que son isótopos. Ambos números conjuntamente determinan el nucleido.
El núcleo atómico puede verse alterado por procesos muy energéticos en comparación con las reacciones químicas. Los núcleos inestables sufren desintegraciones que pueden cambiar su número de protones y neutrones emitiendo radiación. Un núcleo pesado puede fisionarse en otros más ligeros en una reacción nuclear o espontáneamente. Mediante una cantidad suficiente de energía, dos o más núcleos pueden fusionarse en otro más pesado.
En átomos con número atómico bajo, los núcleos con una cantidad distinta de protones y neutrones tienden a desintegrarse en núcleos con proporciones más parejas, más estables. Sin embargo, para valores mayores del número atómico, la repulsión mutua de los protones requiere una proporción mayor de neutrones para estabilizar el núcleo.
Nube de electrones
Los electrones en el átomo son atraídos por los protones a través de la fuerza electromagnética. Esta fuerza los atrapa en un pozo de potencial electrostático alrededor del núcleo, lo que hace necesaria una fuente de energía externa para liberarlos. Cuanto más cerca está un electrón del núcleo, mayor es la fuerza atractiva, y mayor por tanto la energía necesaria para que escape.
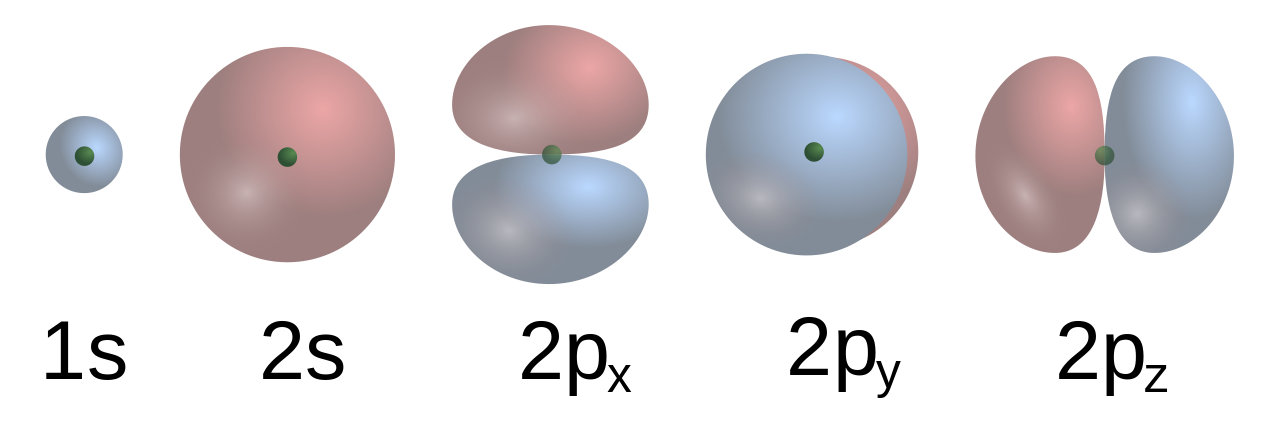
Los electrones, como otras partículas, presentan simultáneamente propiedades de partícula puntual y de onda, y tienden a formar un cierto tipo de onda estacionaria alrededor del núcleo, en reposo respecto de este. Cada una de estas ondas está caracterizada por un orbital atómico, una función matemática que describe la probabilidad de encontrar al electrón en cada punto del espacio. El conjunto de estos orbitales es discreto, es decir, puede enumerarse, como es propio en todo sistema cuántico. La nube de electrones es la región ocupada por estas ondas, visualizada como una densidad de carga negativa alrededor del núcleo.
Cada orbital corresponde a un posible valor de energía para los electrones, que se reparten entre ellos. El principio de exclusión de Pauli prohíbe que más de dos electrones se encuentren en el mismo orbital. Pueden ocurrir transiciones entre los distintos niveles de energía: si un electrón absorbe un fotón con energía suficiente, puede saltar a un nivel superior; también desde un nivel más alto puede acabar en un nivel inferior, radiando el resto de la energía en un fotón. Las energías dadas por las diferencias entre los valores de estos niveles son las que se observan en las líneas espectrales del átomo.
Se denomina isótopos a los átomos de un mismo elemento, cuyos núcleos tienen una cantidad diferente de neutrones, y por lo tanto, difieren en número másico.

La palabra isótopo se usa para indicar que todos los tipos de átomos de un mismo elemento químico (isótopos) se encuentran en el mismo sitio de la tabla periódica. Los átomos que son isótopos entre sí son los que tienen igual número atómico (número de protones en el núcleo), pero diferente número másico (suma del número de neutrones y el de protones en el núcleo). Los distintos isótopos de un elemento difieren, pues, en el número de neutrones.
La mayoría de los elementos químicos tienen más de un isótopo. Solamente 8 elementos (por ejemplo berilio o sodio) poseen un solo isótopo natural. En contraste, el estaño es el elemento con más isótopos estables.
Otros elementos tienen isótopos naturales, pero inestables, como el uranio, cuyos isótopos pueden transformarse o decaer en otros isótopos más estables, emitiendo en el proceso radiación, por lo que se dice que son radiactivos.
Los isótopos inestables son útiles para estimar la edad de una gran variedad de muestras naturales, como rocas y materia orgánica. Esto es posible, siempre y cuando, se conozca el ritmo promedio de desintegración de determinado isótopo, en relación a los que ya han decaído. Gracias a este método de datación, se puede estimar la edad de la Tierra.
La concepción del átomo que se ha tenido a lo largo de la historia ha variado de acuerdo a los descubrimientos realizados en el campo de la física y la química. A continuación se hará una exposición de los modelos atómicos propuestos por los científicos de diferentes épocas. Algunos de ellos son completamente obsoletos para explicar los fenómenos observados actualmente, pero se incluyen a manera de reseña histórica.
Fue el primer modelo atómico con bases científicas, fue formulado en 1803 por John Dalton, quien imaginaba a los átomos como diminutas esferas. Este primer modelo atómico postulaba:
Sin embargo desapareció ante el modelo de Thomson ya que no explica los rayos catódicos, la radioactividad ni la presencia de los electrones (e-) o protones (p+).
Luego del descubrimiento del electrón en 1897 por Joseph John Thomson, se determinó que la materia se componía de dos partes, una negativa y una positiva. La parte negativa estaba constituida por electrones, los cuales se encontraban, según este modelo, inmersos en una masa de carga positiva a manera de pasas en un pastel (de la analogía del inglés plum-pudding model) o uvas en gelatina. Posteriormente Jean Perrin propuso un modelo modificado a partir del de Thomson donde las «pasas» (electrones) se situaban en la parte exterior del «pastel» (protones).

Para explicar la formación de iones, positivos y negativos, y la presencia de los electrones dentro de la estructura atómica, Thomson ideó un átomo parecido a un pastel de frutas. Una nube positiva que contenía las pequeñas partículas negativas (los electrones) suspendidos en ella. El número de cargas negativas era el adecuado para neutralizar la carga positiva. En el caso de que el átomo perdiera un electrón, la estructura quedaría positiva; y si ganaba, la carga final sería negativa. De esta forma, explicaba la formación de iones; pero dejó sin explicación la existencia de las otras radiaciones.
Modelo de Nagaoka
Nagaoka rechazó el modelo de Thomson, debido a que las cargas son impenetrables por la opuesta de cada una. Debido a su disconformidad propuso un modelo alternativo en el que un centro de carga positiva estaba rodeado por un número de electrones que giraban, haciendo el símil con Saturno y sus anillos.
En 1904, Nagaoka desarrolló uno de los primeros modelos planetarios del átomo. Tales como el Modelo atómico de Rutherford. El Modelo de Nagaoka estaba basado alrededor de la analogía con el planeta Saturno, y con las teorías que explicaban la estabilidad y relaciones gravitatorias entre este y sus anillos. La cuestión era esta: los anillos son muy estables porque el planeta que orbitan es muy masivo. Este modelo ofrecía dos predicciones:
Un núcleo muy masivo (en analogía a un planeta muy masivo). Electrones girando alrededor del núcleo atómico, atados a esa órbita por las fuerzas electrostáticas (en analogía a los anillos girando alrededor de Saturno, atados a este por su fuerza gravitatoria).

Este modelo fue desarrollado por el físico Ernest Rutherford a partir de los resultados obtenidos en lo que hoy se conoce como el experimento de Rutherford en 1911. Representa un avance sobre el modelo de Thomson, ya que mantiene que el átomo se compone de una parte positiva y una negativa. Sin embargo, a diferencia del anterior, postula que la parte positiva se concentra en un núcleo, el cual también contiene virtualmente toda la masa del átomo, mientras que los electrones se ubican en una corteza orbitando al núcleo en órbitas circulares o elípticas con un espacio vacío entre ellos. A pesar de ser un modelo obsoleto, es la percepción más común del átomo del público no científico.
Rutherford predijo la existencia del neutrón en el año 1920, por esa razón en el modelo anterior (Thomson), no se habla de este.
Por desgracia, el modelo atómico de Rutherford presentaba varias incongruencias:
Contradecía las leyes del electromagnetismo de James Clerk Maxwell, las cuales estaban muy comprobadas mediante datos experimentales. Según las leyes de Maxwell, una carga eléctrica en movimiento (en este caso el electrón) debería emitir energía constantemente en forma de radiación y llegaría un momento en que el electrón caería sobre el núcleo y la materia se destruiría. Todo ocurriría muy brevemente.
No explicaba los espectros atómicos.
Este modelo es estrictamente un modelo del átomo de hidrógeno tomando como punto de partida el modelo de Rutherford. Niels Bohr trata de incorporar los fenómenos de absorción y emisión de los gases, así como la nueva teoría de la cuantización de la energía desarrollada por Max Planck y el fenómeno del efecto fotoeléctrico observado por Albert Einstein.

«El átomo es un pequeño sistema solar con un núcleo en el centro y electrones moviéndose alrededor del núcleo en órbitas bien definidas». Las órbitas están cuantizadas (los electrones pueden estar solo en ciertas órbitas)
Cada órbita tiene una energía asociada. La más externa es la de mayor energía.
Los electrones no irradian energía (luz) mientras permanezcan en órbitas estables.
Los electrones pueden saltar de una a otra órbita. Si lo hace desde una de menor energía a una de mayor energía absorbe un cuanto de energía (una cantidad) igual a la diferencia de energía asociada a cada órbita. Si pasa de una de mayor a una de menor, pierde energía en forma de radiación (luz).
El mayor éxito de Bohr fue dar la explicación al espectro de emisión del hidrógeno, pero solo la luz de este elemento proporciona una base para el carácter cuántico de la luz, el fotón es emitido cuando un electrón cae de una órbita a otra, siendo un pulso de energía radiada.
Bohr no pudo explicar la existencia de órbitas estables y para la condición de cuantización.
Bohr encontró que el momento angular del electrón es h/2π por un método que no pudo justificar.
El modelo atómico de Bohr funcionaba muy bien para el átomo de hidrógeno, sin embargo, en los espectros realizados para átomos de otros elementos se observaba que electrones de un mismo nivel energético tenían distinta energía, mostrando que existía un error en el modelo. Su conclusión fue que dentro de un mismo nivel energético existían subniveles, es decir, energías ligeramente diferentes.
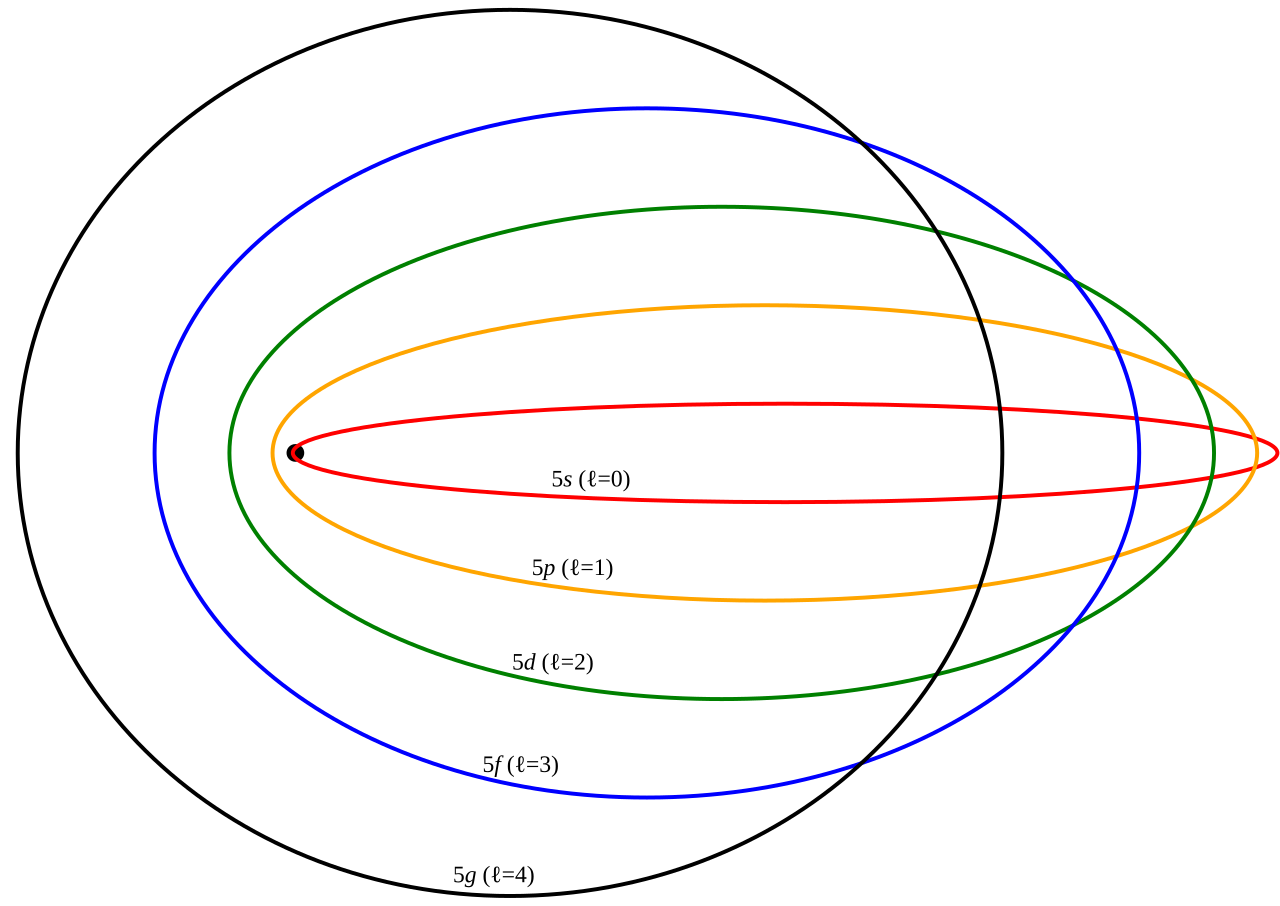
Además desde el punto de vista teórico, Sommerfeld había encontrado que en ciertos átomos las velocidades de los electrones alcanzaban una fracción apreciable de la velocidad de la luz. Sommerfeld estudió la cuestión para electrones relativistas.
El físico alemán finalmente Arnold Sommerfeld, con la ayuda de la teoría de la relatividad de Albert Einstein, hizo las siguientes modificaciones del modelo de Bohr:
Los electrones se mueven alrededor del núcleo, en órbitas circulares o elípticas.
A partir del segundo nivel energético existen dos o más subniveles en el mismo nivel.
El electrón es una corriente eléctrica minúscula.
En consecuencia, el modelo atómico de Sommerfeld es una generalización del modelo atómico de Bohr desde el punto de vista relativista, aunque no pudo demostrar las formas de emisión de las órbitas elípticas, solo descartó su forma circular.

Después de que Louis-Victor de Broglie propuso la naturaleza ondulatoria de la materia en 1924, la cual fue generalizada por Erwin Schrödinger en 1926, se actualizó nuevamente el modelo del átomo.
En el modelo de Schrödinger se abandona la concepción de los electrones como esferas diminutas con carga que giran en torno al núcleo, que es una extrapolación de la experiencia a nivel macroscópico hacia las diminutas dimensiones del átomo. En vez de esto, Schrödinger describe a los electrones por medio de una función de onda, el cuadrado de la cual representa la probabilidad de presencia en una región delimitada del espacio. Esta zona de probabilidad se conoce como orbital. La gráfica siguiente muestra los orbitales para los primeros niveles de energía disponibles en el átomo de hidrógeno.
El modelo de Dirac usa supuestos muy similares al modelo de Schrödinger aunque su punto de partida es una ecuación relativista para la función de onda, la ecuación de Dirac. El modelo de Dirac permite incorporar de manera más natural el espín del electrón. Predice niveles energéticos similares al modelo de Schrödinger proporcionando las correcciones relativistas adecuadas.
Texto:
Imagen:
A pesar de que átomo significa ‘indivisible’, en realidad está formado por varias partículas subatómicas. El átomo contiene protones, neutrones y electrones, con la excepción del átomo de hidrógeno-1, que no contiene neutrones, y del catión hidrógeno o hidrón, que no contiene electrones. Los protones y neutrones del átomo se denominan nucleones, por formar parte del núcleo atómico.

El electrón es la partícula más ligera de las que componen el átomo, con una masa de 9,11 · 10−31 kg. Tiene una carga eléctrica negativa, cuya magnitud se define como la carga eléctrica elemental, y se ignora si posee subestructura, por lo que se considera una partícula elemental. Los protones tienen una masa de 1,672 · 10−24 g, 1836 veces la del electrón, y una carga positiva opuesta a la de este. Los neutrones tienen una masa de 1,69 · 10−27 kg, 1839 veces la del electrón, y no poseen carga eléctrica.
Las masas de ambos nucleones son ligeramente inferiores dentro del núcleo, debido a la energía potencial del mismo, y sus tamaños son similares, con un radio del orden de 8 · 10−16 m o 0,8 femtómetros (fm).
El protón y el neutrón no son partículas elementales, sino que constituyen un estado ligado de quarks u y d, partículas fundamentales recogidas en el modelo estándar de la física de partículas, con cargas eléctricas iguales a +2/3 y −1/3 respectivamente, respecto de la carga elemental. Un protón contiene dos quarks u y un quark d, mientras que el neutrón contiene dos d y un u, en consonancia con la carga de ambos. Los quarks se mantienen unidos mediante la fuerza nuclear fuerte, mediada por gluones —del mismo modo que la fuerza electromagnética está mediada por fotones—. Además de estas, existen otras partículas subatómicas en el modelo estándar: más tipos de quarks, leptones cargados (similares al electrón), etc.
El núcleo atómico
Los protones y neutrones de un átomo se encuentran ligados en el núcleo atómico, en la parte central del mismo. El volumen del núcleo es aproximadamente proporcional al número total de nucleones, el número másico A, lo cual es mucho menor que el tamaño del átomo, cuyo radio es del orden de 105 fm o 1 ángstrom (Å). Los nucleones se mantienen unidos mediante la fuerza nuclear, que es mucho más intensa que la fuerza electromagnética a distancias cortas, lo cual permite vencer la repulsión eléctrica entre los protones.

Los átomos de un mismo elemento tienen el mismo número de protones, que se denomina número atómico y se representa por Z. Los átomos de un elemento dado pueden tener distinto número de neutrones: se dice entonces que son isótopos. Ambos números conjuntamente determinan el nucleido.
El núcleo atómico puede verse alterado por procesos muy energéticos en comparación con las reacciones químicas. Los núcleos inestables sufren desintegraciones que pueden cambiar su número de protones y neutrones emitiendo radiación. Un núcleo pesado puede fisionarse en otros más ligeros en una reacción nuclear o espontáneamente. Mediante una cantidad suficiente de energía, dos o más núcleos pueden fusionarse en otro más pesado.
En átomos con número atómico bajo, los núcleos con una cantidad distinta de protones y neutrones tienden a desintegrarse en núcleos con proporciones más parejas, más estables. Sin embargo, para valores mayores del número atómico, la repulsión mutua de los protones requiere una proporción mayor de neutrones para estabilizar el núcleo.
Nube de electrones
Los electrones en el átomo son atraídos por los protones a través de la fuerza electromagnética. Esta fuerza los atrapa en un pozo de potencial electrostático alrededor del núcleo, lo que hace necesaria una fuente de energía externa para liberarlos. Cuanto más cerca está un electrón del núcleo, mayor es la fuerza atractiva, y mayor por tanto la energía necesaria para que escape.
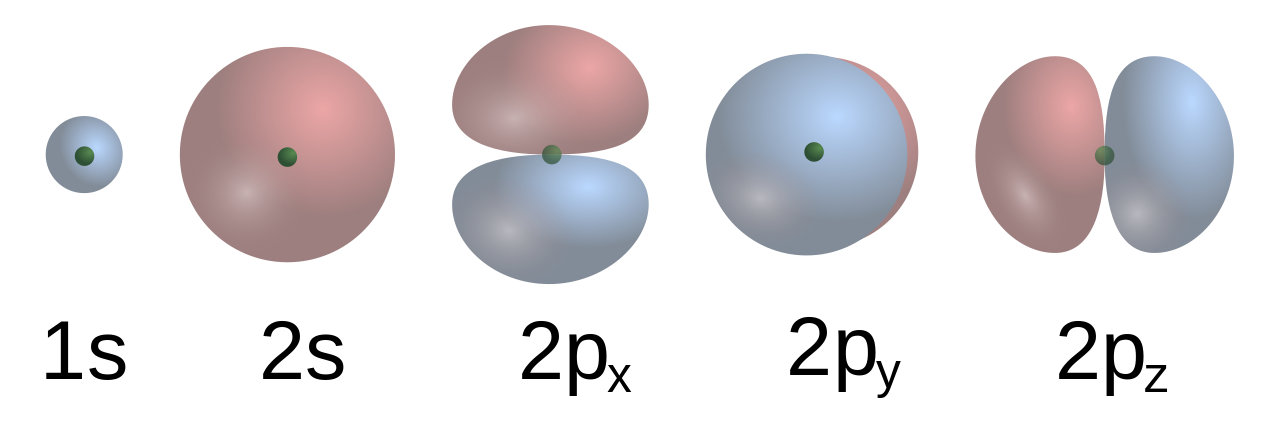
Los electrones, como otras partículas, presentan simultáneamente propiedades de partícula puntual y de onda, y tienden a formar un cierto tipo de onda estacionaria alrededor del núcleo, en reposo respecto de este. Cada una de estas ondas está caracterizada por un orbital atómico, una función matemática que describe la probabilidad de encontrar al electrón en cada punto del espacio. El conjunto de estos orbitales es discreto, es decir, puede enumerarse, como es propio en todo sistema cuántico. La nube de electrones es la región ocupada por estas ondas, visualizada como una densidad de carga negativa alrededor del núcleo.
Cada orbital corresponde a un posible valor de energía para los electrones, que se reparten entre ellos. El principio de exclusión de Pauli prohíbe que más de dos electrones se encuentren en el mismo orbital. Pueden ocurrir transiciones entre los distintos niveles de energía: si un electrón absorbe un fotón con energía suficiente, puede saltar a un nivel superior; también desde un nivel más alto puede acabar en un nivel inferior, radiando el resto de la energía en un fotón. Las energías dadas por las diferencias entre los valores de estos niveles son las que se observan en las líneas espectrales del átomo.
Se denomina isótopos a los átomos de un mismo elemento, cuyos núcleos tienen una cantidad diferente de neutrones, y por lo tanto, difieren en número másico.

La palabra isótopo se usa para indicar que todos los tipos de átomos de un mismo elemento químico (isótopos) se encuentran en el mismo sitio de la tabla periódica. Los átomos que son isótopos entre sí son los que tienen igual número atómico (número de protones en el núcleo), pero diferente número másico (suma del número de neutrones y el de protones en el núcleo). Los distintos isótopos de un elemento difieren, pues, en el número de neutrones.
La mayoría de los elementos químicos tienen más de un isótopo. Solamente 8 elementos (por ejemplo berilio o sodio) poseen un solo isótopo natural. En contraste, el estaño es el elemento con más isótopos estables.
Otros elementos tienen isótopos naturales, pero inestables, como el uranio, cuyos isótopos pueden transformarse o decaer en otros isótopos más estables, emitiendo en el proceso radiación, por lo que se dice que son radiactivos.
Los isótopos inestables son útiles para estimar la edad de una gran variedad de muestras naturales, como rocas y materia orgánica. Esto es posible, siempre y cuando, se conozca el ritmo promedio de desintegración de determinado isótopo, en relación a los que ya han decaído. Gracias a este método de datación, se puede estimar la edad de la Tierra.
La concepción del átomo que se ha tenido a lo largo de la historia ha variado de acuerdo a los descubrimientos realizados en el campo de la física y la química. A continuación se hará una exposición de los modelos atómicos propuestos por los científicos de diferentes épocas. Algunos de ellos son completamente obsoletos para explicar los fenómenos observados actualmente, pero se incluyen a manera de reseña histórica.

Fue el primer modelo atómico con bases científicas, fue formulado en 1803 por John Dalton, quien imaginaba a los átomos como diminutas esferas. Este primer modelo atómico postulaba:
Sin embargo desapareció ante el modelo de Thomson ya que no explica los rayos catódicos, la radioactividad ni la presencia de los electrones (e-) o protones (p+).
Luego del descubrimiento del electrón en 1897 por Joseph John Thomson, se determinó que la materia se componía de dos partes, una negativa y una positiva. La parte negativa estaba constituida por electrones, los cuales se encontraban, según este modelo, inmersos en una masa de carga positiva a manera de pasas en un pastel (de la analogía del inglés plum-pudding model) o uvas en gelatina. Posteriormente Jean Perrin propuso un modelo modificado a partir del de Thomson donde las «pasas» (electrones) se situaban en la parte exterior del «pastel» (protones).

Para explicar la formación de iones, positivos y negativos, y la presencia de los electrones dentro de la estructura atómica, Thomson ideó un átomo parecido a un pastel de frutas. Una nube positiva que contenía las pequeñas partículas negativas (los electrones) suspendidos en ella. El número de cargas negativas era el adecuado para neutralizar la carga positiva. En el caso de que el átomo perdiera un electrón, la estructura quedaría positiva; y si ganaba, la carga final sería negativa. De esta forma, explicaba la formación de iones; pero dejó sin explicación la existencia de las otras radiaciones.
Modelo de Nagaoka
Nagaoka rechazó el modelo de Thomson, debido a que las cargas son impenetrables por la opuesta de cada una. Debido a su disconformidad propuso un modelo alternativo en el que un centro de carga positiva estaba rodeado por un número de electrones que giraban, haciendo el símil con Saturno y sus anillos.
En 1904, Nagaoka desarrolló uno de los primeros modelos planetarios del átomo. Tales como el Modelo atómico de Rutherford. El Modelo de Nagaoka estaba basado alrededor de la analogía con el planeta Saturno, y con las teorías que explicaban la estabilidad y relaciones gravitatorias entre este y sus anillos. La cuestión era esta: los anillos son muy estables porque el planeta que orbitan es muy masivo. Este modelo ofrecía dos predicciones:
Un núcleo muy masivo (en analogía a un planeta muy masivo). Electrones girando alrededor del núcleo atómico, atados a esa órbita por las fuerzas electrostáticas (en analogía a los anillos girando alrededor de Saturno, atados a este por su fuerza gravitatoria).

Este modelo fue desarrollado por el físico Ernest Rutherford a partir de los resultados obtenidos en lo que hoy se conoce como el experimento de Rutherford en 1911. Representa un avance sobre el modelo de Thomson, ya que mantiene que el átomo se compone de una parte positiva y una negativa. Sin embargo, a diferencia del anterior, postula que la parte positiva se concentra en un núcleo, el cual también contiene virtualmente toda la masa del átomo, mientras que los electrones se ubican en una corteza orbitando al núcleo en órbitas circulares o elípticas con un espacio vacío entre ellos. A pesar de ser un modelo obsoleto, es la percepción más común del átomo del público no científico.
Rutherford predijo la existencia del neutrón en el año 1920, por esa razón en el modelo anterior (Thomson), no se habla de este.
Por desgracia, el modelo atómico de Rutherford presentaba varias incongruencias:
Contradecía las leyes del electromagnetismo de James Clerk Maxwell, las cuales estaban muy comprobadas mediante datos experimentales. Según las leyes de Maxwell, una carga eléctrica en movimiento (en este caso el electrón) debería emitir energía constantemente en forma de radiación y llegaría un momento en que el electrón caería sobre el núcleo y la materia se destruiría. Todo ocurriría muy brevemente.
No explicaba los espectros atómicos.
Este modelo es estrictamente un modelo del átomo de hidrógeno tomando como punto de partida el modelo de Rutherford. Niels Bohr trata de incorporar los fenómenos de absorción y emisión de los gases, así como la nueva teoría de la cuantización de la energía desarrollada por Max Planck y el fenómeno del efecto fotoeléctrico observado por Albert Einstein.

«El átomo es un pequeño sistema solar con un núcleo en el centro y electrones moviéndose alrededor del núcleo en órbitas bien definidas». Las órbitas están cuantizadas (los electrones pueden estar solo en ciertas órbitas)
Cada órbita tiene una energía asociada. La más externa es la de mayor energía.
Los electrones no irradian energía (luz) mientras permanezcan en órbitas estables.
Los electrones pueden saltar de una a otra órbita. Si lo hace desde una de menor energía a una de mayor energía absorbe un cuanto de energía (una cantidad) igual a la diferencia de energía asociada a cada órbita. Si pasa de una de mayor a una de menor, pierde energía en forma de radiación (luz).
El mayor éxito de Bohr fue dar la explicación al espectro de emisión del hidrógeno, pero solo la luz de este elemento proporciona una base para el carácter cuántico de la luz, el fotón es emitido cuando un electrón cae de una órbita a otra, siendo un pulso de energía radiada.
Bohr no pudo explicar la existencia de órbitas estables y para la condición de cuantización.
Bohr encontró que el momento angular del electrón es h/2π por un método que no pudo justificar.
El modelo atómico de Bohr funcionaba muy bien para el átomo de hidrógeno, sin embargo, en los espectros realizados para átomos de otros elementos se observaba que electrones de un mismo nivel energético tenían distinta energía, mostrando que existía un error en el modelo. Su conclusión fue que dentro de un mismo nivel energético existían subniveles, es decir, energías ligeramente diferentes.

Además desde el punto de vista teórico, Sommerfeld había encontrado que en ciertos átomos las velocidades de los electrones alcanzaban una fracción apreciable de la velocidad de la luz. Sommerfeld estudió la cuestión para electrones relativistas.
El físico alemán finalmente Arnold Sommerfeld, con la ayuda de la teoría de la relatividad de Albert Einstein, hizo las siguientes modificaciones del modelo de Bohr:
Los electrones se mueven alrededor del núcleo, en órbitas circulares o elípticas.
A partir del segundo nivel energético existen dos o más subniveles en el mismo nivel.
El electrón es una corriente eléctrica minúscula.
En consecuencia, el modelo atómico de Sommerfeld es una generalización del modelo atómico de Bohr desde el punto de vista relativista, aunque no pudo demostrar las formas de emisión de las órbitas elípticas, solo descartó su forma circular.

Después de que Louis-Victor de Broglie propuso la naturaleza ondulatoria de la materia en 1924, la cual fue generalizada por Erwin Schrödinger en 1926, se actualizó nuevamente el modelo del átomo.
En el modelo de Schrödinger se abandona la concepción de los electrones como esferas diminutas con carga que giran en torno al núcleo, que es una extrapolación de la experiencia a nivel macroscópico hacia las diminutas dimensiones del átomo. En vez de esto, Schrödinger describe a los electrones por medio de una función de onda, el cuadrado de la cual representa la probabilidad de presencia en una región delimitada del espacio. Esta zona de probabilidad se conoce como orbital. La gráfica siguiente muestra los orbitales para los primeros niveles de energía disponibles en el átomo de hidrógeno.
El modelo de Dirac usa supuestos muy similares al modelo de Schrödinger aunque su punto de partida es una ecuación relativista para la función de onda, la ecuación de Dirac. El modelo de Dirac permite incorporar de manera más natural el espín del electrón. Predice niveles energéticos similares al modelo de Schrödinger proporcionando las correcciones relativistas adecuadas.
Texto:
Imagen:
Contenido exclusivo para miembros de
Mira un ejemplo de lo que te pierdes
Categorías:
Etiquetas:
¿Quieres comentar? Regístrate o inicia sesión
Si ya eres usuario, Inicia sesión
Añadir a Didactalia Arrastra el botón a la barra de marcadores del navegador y comparte tus contenidos preferidos. Más info...
Comentar
0