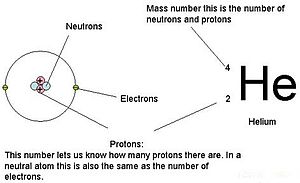
Il numero atomico (indicato solitamente con Z, dal tedesco Zahl, e detto anche numero protonico) corrisponde al numero di protoni contenuti in un nucleo atomico.In un atomo neutro il numero atomico è pari anche al numero di elettroni; in caso contrario l'atomo è detto ione.Si usa scrivere questo numero come pedice sinistro del simbolo dell'elemento chimico in questione: per esempio 6C, poiché il carbonio ha sei protoni.A ogni numero atomico corrisponde un diverso elemento chimico, il quale viene collocato nella tavola periodica proprio in funzione del relativo valore di Z. La legge di Moseley permette di ricavare il numero atomico di un dato elemento misurando la frequenza della riga caratteristica corrispondente all'emissione di raggi X.Atomi aventi stesso numero atomico ma diverso numero di neutroni sono detti isotopi.Secondo la teoria di Niels Bohr, in cui il numero di elettroni aumenta con l'aumentare del numero degli orbitali (k = 2 × 12 = 2; l = 2 × 22 = 8; m = 2 × 32 = 18), anche la forma della tavola periodica dovrebbe cambiare. Questa teoria porrebbe fine anche al problema della collocazione delle terre rare. Per determinare il numero degli elementi contenuti nel proprio periodo, bisogna considerare il numero atomico dei gas nobili, pari a:2, 10, 18, 36, 54, 86, 118.e fare la differenza tra due gas adiacenti:10 − 2 = 8; 18 − 10 = 8; 36 − 18 = 18; 54 − 36 = 18; 86 − 54 = 32; 118 − 86 = 32Si noti che il risultato è identico al risultato delle moltiplicazioni sopra scritte e che si ripete 2 volte prima di cambiare.In questo modo si capisce il perché dei "salti di due caselle": dopo l'elio si salta, poi ci sono due periodi che combaciano (2 e 3), poi ci sono i metalli di transizione (4 e 5), le terre rare (6 e 7). In tal modo si può anche scoprire il numero atomico del prossimo gas nobile, 118 + (2 × 52) = 168.


Commenta
0